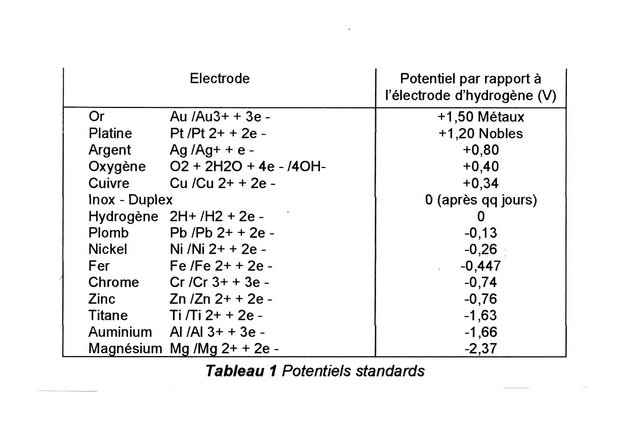
Phénomène électrolytique entre cuivre et fer pur
Bonjour,
j'ai proposé à un client un garde corps en fer pur riveté avec rivets cuivre. Ce même client s'avère avoir des connaissances en chimie et me parle du phénomène électrolytique entre métaux. Je ne pensais jusqu'alors pas qu'il était assez important pour le proscrire dans le cas du cuivre et du fer pur même en extérieur étant entendu que le fer pur s'oxyde mais ne corrode pas.
D'où mes questions :
- Quelle est l'importance de la dégradation électrolytique du fer pur par son assemblage avec du cuivre, dans le cas d'une pose de cet ensemble à l'extérieur ?
- L'utilisation d'acier ou de fer doux serait-elle plus judicieuse ?
Merci pour vos réponses.
j'ai proposé à un client un garde corps en fer pur riveté avec rivets cuivre. Ce même client s'avère avoir des connaissances en chimie et me parle du phénomène électrolytique entre métaux. Je ne pensais jusqu'alors pas qu'il était assez important pour le proscrire dans le cas du cuivre et du fer pur même en extérieur étant entendu que le fer pur s'oxyde mais ne corrode pas.
D'où mes questions :
- Quelle est l'importance de la dégradation électrolytique du fer pur par son assemblage avec du cuivre, dans le cas d'une pose de cet ensemble à l'extérieur ?
- L'utilisation d'acier ou de fer doux serait-elle plus judicieuse ?
Merci pour vos réponses.